Liens entre Atomes :
Dans cette leçon, nous commencerons à nous occuper des semi-conducteurs, matériaux
qui ont permis de réaliser d'importants dispositifs (diodes, transistors, circuits intégrés...) en mesure d'assurer des fonctions multiples et complexes.
Pour comprendre parfaitement le fonctionnement des dispositifs à semi-conducteurs, il est nécessaire de bien connaître la structure des matériaux utilisés pour leur fabrication. Nous commencerons par un rapide examen de la structure interne des cristaux. Tout au long de ce développement, on aura souvent recours à des figures pour représenter d'une façon analogique les phénomènes
qui se produisent dans les semi-conducteurs. Le recours à ces figures est très utile toutes les fois qu'il n'est pas possible de visualiser directement le phénomène
à étudier. Même si cette représentation est toujours approximative et ne reproduit pas fidèlement le phénomène, elle peut toutefois, d'une certaine façon
et pour un temps donné, représenter du mieux possible les phénomènes connus. Toutes les expériences de chimie démontrent que les atomes de corps différents, s'attirent ou se repoussent, lorsqu'ils sont
placés à petite distance les uns des autres. Il faut préciser tout de suite que lorsqu'il s'agit de distance entre atomes, on utilise comme unité de mesure l'angström
(symbole Å ) équivalent au dix millionième de millimètre ou le millimicron (symbole mµ)
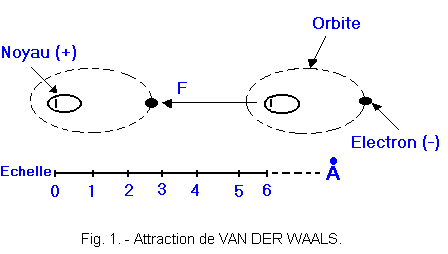
correspondant au millionième de millimètre. L'attraction qui se manifeste entre les atomes est appelée attraction de VAN DER WAALS ;
elle est en général relativement faible et ne commence à s'exercer que lorsque les atomes sont à des distances de quelques angströms (figure 1). A plus faible distance, lorsque les orbites externes des électrons se
touchent, il peut s'établir un lien plus étroit, appelé lien chimique, ou au contraire il peut se produire une force répulsion. L'attraction de VAN DER WAALS est essentiellement un phénomène de nature électrostatique, dû à la force électrique
d'attraction, s'exerçant entre le noyau électriquement positif et les électrons de l'atome voisin, électriquement négatifs. Le lien chimique et la répulsion sont au contraire dus à la constitution de la dernière couche des électrons, tournant
autour du noyau, c'est-à-dire la couche externe. En général, les couches internes des électrons sont stables et ne sont pas concernées par les phénomènes
chimiques et électriques. La couche externe au contraire peut présenter une certaine instabilité, car elle peut perdre ou gagner des électrons ou
encore les mettre en commun avec les électrons de la couche externe d'un atome voisin. Pour expliquer la formation du lien chimique dans certains cas et dans d'autres la répulsion, il faut se référer à un principe
physique, connu sous le nom de principe de PAULI. D'après ce principe, dans
chaque orbite électronique placée autour du noyau d'un atome, il ne peut y avoir qu'un électron ayant une énergie déterminée. Cependant, si
l'on admet que tous les électrons sont exactement égaux entre eux et, qu'un électron sur son orbite tourne aussi sur lui-même dans un sens ou dans l'autre, on peut
modifier l'expression précédente du principe de PAULI et écrire : sur l'orbite d'un noyau, il ne peut tourner plus de deux électrons et ces derniers
tournant sur eux-mêmes, doivent tourner en sens inverse l'un de l'autre (principe de PAULI généralisé sur lequel nous nous baserons dans les
explications qui suivent). Nous admettrons ce principe sans le démontrer car il nécessite des connaissances très profondes en physique nucléaire
sortant du cadre de cette leçon. Imaginons maintenant que deux atomes d'hydrogène se rapprochent l'un de l'autre. On peut représenter les atomes de l'hydrogène
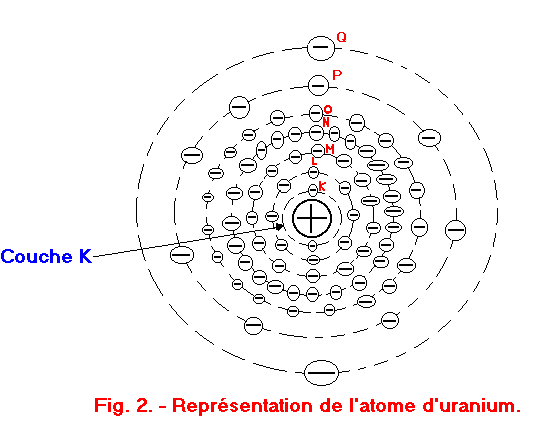
comme sur la figure 1 ; ils sont constitués d'un noyau et d'un seul électron tournant sur la couche
K (figure 2 : atome d'uranium comportant ici, 7 couches sur lesquelles gravitent des électrons ; la couche K dispose de 2 électrons dans cet exemple). Lorsque les noyaux des deux atomes se trouvent à une distance de quelques angströms (5 Å environ), l'attraction de VAN DER
WAALS commence à se manifester. Si la distance diminue, l'attraction électrostatique augmente et à partir de 0,75 Å, le lien
chimique intervient. Ce lien assure l'union stable des deux atomes et détermine ainsi la formation de la molécule d'hydrogène. Le lien chimique n'est pas uniquement constitué par une forte attraction électrostatique entre le noyau et les électrons, mais
aussi par un échange d'énergie entre les atomes, échange se produisant par l'intermédiaire des électrons passant successivement et indifféremment de
l'orbite d'un atome à l'orbite d'un autre atome. Lors du continuel passage des électrons d'un atome à l'autre, il arrive évidemment que sur l'orbite d'un atome d'hydrogène
il se trouve deux électrons au lieu d'un. Cette possibilité est évoquée dans le principe de PAULI généralisé puisque dans chaque orbite on peut trouver deux électrons. Considérons maintenant un autre cas : imaginons que deux atomes d'hélium se sont
rapprochés l'un de l'autre. Les atomes d'hélium sont constitués d'un noyau et de deux électrons gravitant sur la couche K. Cette couche, c'est-à-dire la
couche la plus proche du noyau est constituée d'une seule orbite. Pour l'hélium, cette couche est complète, car elle comprend deux électrons et ne peut, d'après le principe de PAULI en
accueillir d'autres. Lorsque les noyaux des deux atomes d'hélium se trouvent à une distance de quelques angströms, l'attraction de VAN DER WAALS
peut se manifester ; toutefois à une distance plus faible, il se produit une forte répulsion au lieu du lien chimique. Cette répulsion entre les deux
atomes d'hélium est due aux interaction de leurs électrons. En effet, nous savons que les électrons ont tous la même charge et qu'ils se repoussent entre
eux. D'autre part, il est impossible d'obtenir une répartition stable des électrons autour des deux noyaux comme dans le cas de l'hydrogène, car d'après le
principe de PAULI généralisé, l'orbite de chaque atome d'hélium est considérée comme complète. Nous n'avons jusqu'ici examiné que des atomes simples, ne comportant qu'une seule couche d'électrons, la couche K. Dans le cas d'atomes à deux ou plusieurs couches (figure 2), il faut non seulement tenir compte du principe de PAULI mais aussi
du fait que la stabilité maximale des électrons est obtenue, lorsque la couche externe comprend huit électrons gravitant sur
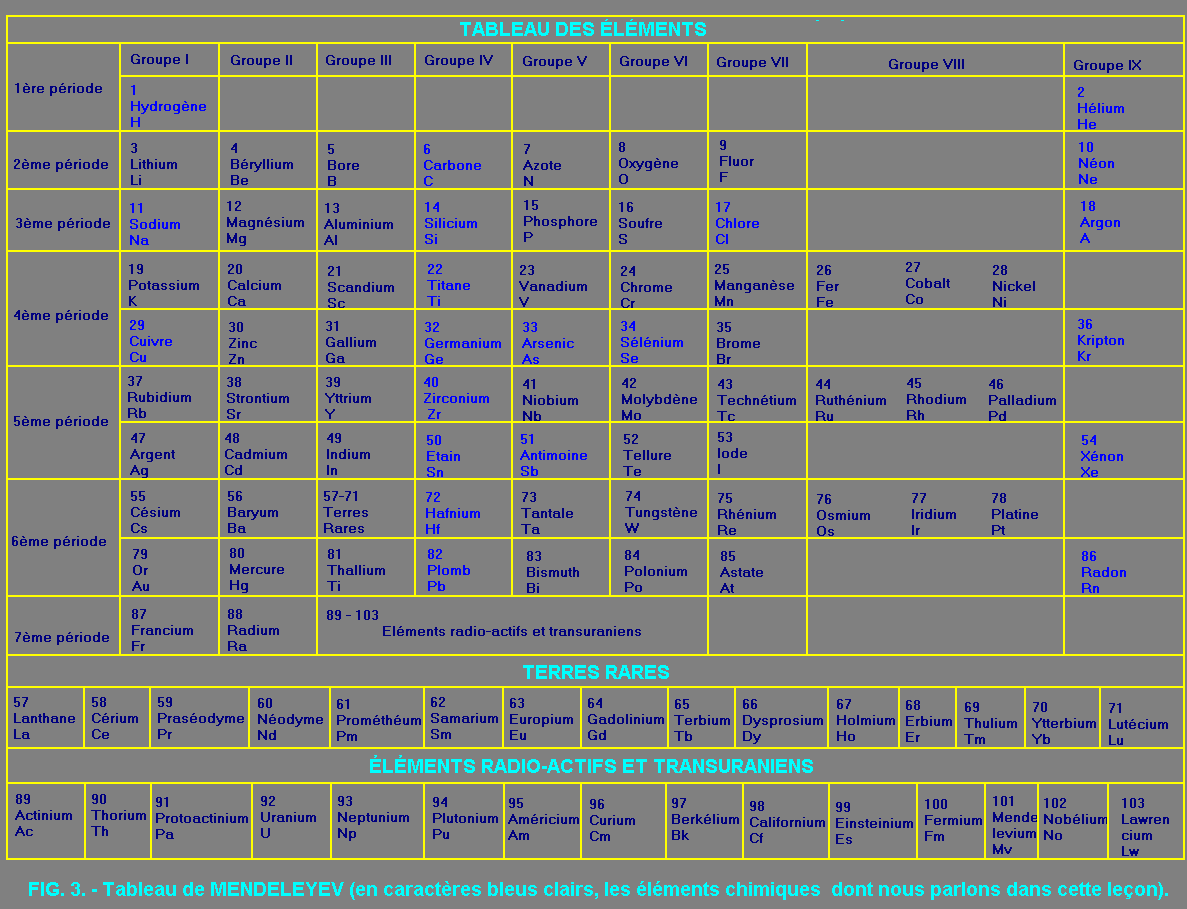
quatre orbites. Les éléments ayant huit électrons, sur la couche externe sont réunis dans le groupe IX du tableau de MENDELEYEV donné
figure 3. Par contre, si un atome à moins de huit électrons dans une couche externe, différente de la couche K, il aura tendance à
accepter le lien chimique avec d'autres atomes. Cette capacité de l'atome de se lier chimiquement avec d'autres atomes est dite valence.
Il existe une certaine relation entre la valence d'un atome et le nombre d'électrons qui comprend sa couche externe. - Lorsque la couche externe est complète avec huit électrons, on dit que l'atome à une valence zéro.
- Lorsque la couche externe ne comprend qu'un seul électron, ou sept électrons, on dit que l'atome à une valence
un ou encore qu'il est monovalent.
- Lorsque la couche externe ne comprend que
deux électrons ou six électrons, on dit que l'atome à la valence
deux ou encore qu'il est bivalent.
- Lorsque la couche externe ne comprend que
trois électrons ou cinq électrons, on dit que l'atome à la valence
trois ou encore qu'il est trivalent.
- Enfin, si la couche externe ne comprend que
quatre électrons, on dit que l'atome à la valence
quatre ou encore qu'il est tétravalent.
Ce critère pour distinguer les valences n'est cependant pas toujours valable ; il y a même de nombreuses exceptions. Par exemple, l'antimoine, l'arsenic et le phosphore
ne possèdent que cinq électrons sur leur couche externe et peuvent par conséquent être trivalents d'après le critère
ci-dessus, mais peuvent également avoir une valence cinq. Dans ce cas, ils sont
dits pentavalents. On trouve aussi des atomes pouvant avoir une valence six (hexavalents) et une valence
sept (heptavalents). Il n'est pas nécessaire d'approfondir le concept
général de valence, concept lié à des recherches très complexes sortant du cadre de cette leçon, mais il est utile par contre de bien mettre en évidence
le lien chimique entre les atomes d'un même élément. Nous avons précédemment considéré le lien qui s'établit entre deux atomes d'hydrogène, lorsque leurs noyaux respectifs se
trouvent à une distance de 0,75Å. Ce type particulier de lien chimique entre atomes de la même espèce est dit lien covalent ou
encore lien homopolaire. Voyons comment peut s'établir un lien covalent entre atomes, ayant plus de deux électrons et moins de huit dans leur couche externe. Prenons par exemple quelques atomes d'un élément tétravalent, c'est-à-dire un élément possédant quatre électrons sur sa
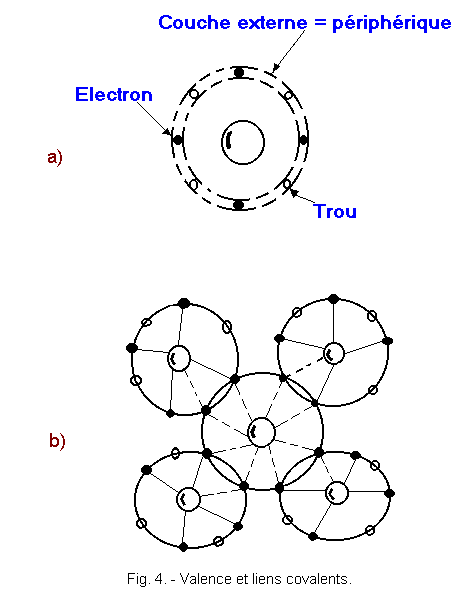
couche périphérique. Pour simplifier la représentation, on a fait figurer sur le dessin de la figure 4-a que le noyau des atomes et les quatre électrons
périphériques (les électrons des autres couches n'étant pas concernés). Bien entendu, en réalité les quatre électrons périphériques de chaque atome, occupent plusieurs orbites, mais pour plus de
clarté il suffit de n'en représenter qu'une seule. Entre les électrons périphériques, on a aussi dessiné quatre trous, qui représentent les
places libres, dans lesquelles pourraient venir quatre autres électrons, de façon à compléter la couche externe. Le croquis de la figure 4-a peut représenter tous les atomes des éléments tétravalents classés dans le groupe IV du
tableau de MENDELEYEV (figure 3), c'est-à-dire le carbone, le silicium, le titane, le germanium, le zirconium,
l'étain, l'hafnium et le plomb. Imaginons maintenant que quatre atomes tétravalents se rapprochent d'un atome du même type. Lorsque ces atomes se trouvent à
quelques angströms, les forces de VAN DER WAALS se manifestent ; mais à de plus faibles distances il s'établit un lien covalent entre l'atome considéré
et chacun des quatre atomes qui se sont rapprochés. Les quatre liens covalents sont représentés figure 4-b par les quatre rayons en pointillés. Ce phénomène est facile à
comprendre. En effet, au centre nous avons un atome instable avec quatre électrons sur la couche externe qui peut soit en récupérer, soit en céder. A proximité de ces atomes, quatre autres atomes du même type se sont rapprochés jusqu'à ce que les orbites soient en contact
les unes avec les autres. Tout naturellement l'atome du centre comble donc ses quatre trous (voir figure 4-a) avec les électrons instables des quatre autres atomes. L'atome du centre a ainsi sa couche externe complète avec huit électrons. En réalité, ces huit électrons n'appartiennent pas
exclusivement au même atome ; ils se subdivisent en quatre couples et chaque couple d'électrons appartient manifestement à l'atome central et à un
atome périphérique. Le lien covalent, existant entre l'atome central et les quatre atomes périphériques, consiste en un échange répété d'énergie
dû au passage d'électrons d'un atome à l'autre.
Envoyez un courrier électronique à Administrateur Web Société pour toute question ou remarque concernant ce site Web.
Version du site : 10. 5. 14 - Site optimisation 1280 x 1024 pixels - Faculté de Nanterre - Dernière modification : 22 MAI 2023.
Ce site Web a été Créé le, 14 Mars 1999 et ayant Rénové, en MAI 2023.
![]() 1. - LIENS ENTRE ATOMES :
1. - LIENS ENTRE ATOMES :
 Cliquez ici pour la leçon suivante ou dans le sommaire prévu à cet effet.
Cliquez ici pour la leçon suivante ou dans le sommaire prévu à cet effet.
Haut de page
 Page précédente
Page précédente
 Page suivante
Page suivante
Nombre de pages vues, à partir de cette date : le 23 MAI 2019
 Liens entre atomes
Liens entre atomes